In diesem Beitrag erfährst Du alles Wichtige über die Corona Impfung sowie die häufigsten Fragen über die verschiedenen Impfungen, Inhaltsstoffe, Nebenwirkungen und Effektivität. Dieser Artikel ist auf dem aktuellsten wissenschaftlichen und medizinischen Stand (April, 2021).
Der heutige Beitrag ist in Zusammenarbeit mit Dr. med. Elke Lenhart entstanden. Elke ist Fachärztin für Gynäkologie und Geburtshilfe und Impfärztin für die aktuelle Impfkampagne gegen Covid-19 in Schleswig-Holstein.
Vielen Dank an Elke an dieser Stelle!
Dieser Beitrag gehört zu den ausführlichsten Berichten über die Corona Impfung im deutschsprachigen Raum und ist an den aktuellsten wissenschaftlichen und medizinischen Studien und Erfahrungen orientiert.
Impfen ist nicht so ein Schwarz-Weiß-Thema, wie es oft dargestellt wird. Jede Impfung sollte individuell betrachtet werden – manche machen allgemein gesehen Sinn und sind sicher, andere weniger. Zudem sollte eine Impfung bei jeder Person individuell betrachtet und abgewogen werden.
So gesehen, ist kein Impfstoff immer nur gut oder nur schlecht.
Bei der Corona Impfung ist es genauso – die verschiedenen Impfstoffe haben unterschiedliche Vor- und Nachteile und eignen sich für unterschiedliche Personengruppen mehr oder weniger gut. Wer für sich Vorteile durch eine Impfung sieht, soll hier Aufklärung erhalten. Wer sich noch nicht sicher ist oder noch Fragen hat, wird hier auch Antworten bekommen.
In diesem Beitrag werden auch immer die Vor- und Nachteile diskutiert, so dass sich jeder selbst eine Meinung bilden kann.
Relativ nüchtern und un-emotional – und das ist wichtig, da die Corona Impfung für viele zur Glaubensfrage mutiert ist. Das wollen wir hier ändern.
Den Umgang politischer Entscheidungsträger mit der aktuellen Pandemie (z.B. Lockdowns) wollen wir mit diesem Beitrag nicht thematisieren oder bewerten.
Und noch etwas: Ob mit oder ohne Impfung – ein gesundes und robustes Immunsystem ist für Jedermann relevant – dafür setzen wir uns bei SchnellEinfachGesund auch ein und gehen gegen Ende des Beitrags darauf ein.
Inhaltsverzeichnis
- 1 Über die Autorin, Dr. med. Elke Lenhart
- 2 Alles Wichtige über die Corona Impfung
- 2.1 Welche Impfstoffe stehen uns aktuell zum Schutz vor COVID-19 zur Verfügung?
- 2.2 Wie funktionieren diese neu entwickelten Impfstoffe?
- 2.3 Können diese gentechnisch hergestellten Impfstoffe das menschliche Erbgut beeinflussen?
- 2.4 Was ist mit den Vektorimpfstoffen? Könnten diese unser Erbgut beeinflussen?
- 2.5 Enthalten die bisher zugelassenen COVID-19-Impfstoffe problematische Inhaltsstoffe wie Quecksilber, Aluminium oder Formaldehyd?
- 2.6 Sind diese Impfstoffe in Studien ausreichend getestet – oder handelt es sich eigentlich gerade um ein großes Experiment?
- 2.7 Gibt es Unterschiede bei der Wirksamkeit der einzelnen Impfstoffe?
- 2.8 Schützen die Impfstoffe auch vor den neuen Covid-Mutanten?
- 2.9 Wie lange hält die Schutzwirkung der Impfungen an?
- 2.10 Welche Nebenwirkungen können im Zusammenhang mit einer COVID-19-Impfung auftreten?
- 2.11 Sind Langzeitfolgen wie Autoimmunerkrankungen oder Krebs möglich?
- 2.12 Lass uns noch die häufigsten Fake News in Zusammenhang mit den COVID-19 Impfungen besprechen. Stimmt es, dass die Impfung unfruchtbar macht?
- 2.13 Stimmt es, dass die COVID-19-Impfungen Lungenentzündungen verursachen?
- 2.14 Stimmt es, dass die COVID-19-Impfstoffe Mikro- oder Nanochips enthalten?
- 2.15 Wer sollte sich nicht impfen lassen oder besondere Vorsichtsmaßnahmen treffen?
- 2.16 Muss ich mich impfen lassen?
- 2.17 Kann ich mich impfen lassen?
- 2.18 Soll ich mich impfen lassen?
- 2.19 Wie kann ich mich auf die Impfung vorbereiten, um das Ansprechen zu erhöhen und Nebenwirkungen erträglicher zu machen?
- 2.20 Wo kann ich weitere Informationen finden?
Über die Autorin, Dr. med. Elke Lenhart
Elke Lenhart studierte Humanmedizin an der RWTH Aachen und war während des Studiums als medizinische Doktorandin am Institut für Humangenetik im Forschungsprojekt „Molekulargenetische Grundlagen der Präeklampsie“ tätig. Nach ihrer Promotion absolvierte sie ihre Facharztweiterbildung in Gynäkologie und Geburtshilfe in der Schweiz und in der Asklepios Klinik Barmbek in Hamburg.
Heute arbeitet sie hauptberuflich als ärztliche Beraterin und Gutachterin für sozialmedizinische Fragestellungen. Im Rahmen der aktuellen Impfkampagne gegen Covid-19 arbeitet sie nebenberuflich in den drei Impfzentren Bad Oldesloe, Reinbek und Großhansdorf im Kreis Stormarn in Schleswig-Holstein. Sie ist 42 Jahre alt und lebt mit ihrem Mann und ihren drei Kindern in Hamburg.
Liebe Elke: Bevor wir gleich auf die inhaltlichen Fragen zum Thema COVID-19-Impfungen eingehen, hätte ich noch drei kurze Fragen an Dich:
Alles Wichtige über die Corona Impfung
Im Anschluss findest Du die wichtigsten Fragen zur Corona Impfung mit den Antworten von Dr. Elke Lenhart:
Welche Impfstoffe stehen uns aktuell zum Schutz vor COVID-19 zur Verfügung?
Aktuell werden in Deutschland ganz überwiegend die Impfstoffe Comirnaty® von BioNTech/Pfizer und Vaxzevria® von AstraZeneca verimpft. Das Covid-19 Vaccine Moderna® wird bei uns nur in sehr geringem Umfang geliefert.
Das Covid-19 Vaccine Janssen® von Johnson & Johnson ist seit dem 11.03.2021 zugelassen und wird seit dem 01.04.2021 von der STIKO für alle Altersgruppen ab 18 Jahre empfohlen.
Weitere Impfstoffkandidaten der Firmen CureVac und Novavax sowie Sputnik V® werden z. Zt. von der Europäischen Arzneimittelagentur EMA geprüft. Die Zulassung wird für Mai oder Juni erwartet.
Wie funktionieren diese neu entwickelten Impfstoffe?
Neu ist, dass die COVID-19-Impfstoffe nicht mehr das Antigen selbst, sondern die genetische Information für das Antigen enthalten und damit die geimpfte Zelle dazu veranlassen, das Antigen herstellen.
Als Antigen nutzen die Impfstoffe das S-Protein (Spike protein), den „Stachel“ auf der Oberfläche der Coronaviren, mit dem sie an den Rezeptor der Wirtszelle binden.
Dabei unterscheiden sich die Impfstoffe im Transportmedium der genetischen Information für das S-Protein: mRNA-Impfstoffe nutzen eine Lipidhülle für den Transport in die Zelle hinein, Vektor-Impfstoffe nutzen ein gentechnisch modifiziertes Virus als Vektor.
Das Immunsystem reagiert auf das S-Protein als Antigen und bildet mit Hilfe von B-Zellen schützende Antikörper, aber auch Abwehrzellen in Form von spezifischen zytotoxischen T-Zellen. Bei einer Ansteckung mit SARS-CoV-2 werden diese Zellen wieder aktiviert, um eine Infektion abzuwehren.
Wenn man den Wirkmechanismus im Detail nachvollziehen möchte, muss man sich mit den Prozessen der Proteinbiosynthese auseinandersetzen. mRNA-Impfstoffe enthalten einen modifizierten Abschnitt aus dem RNA-Genom von SARS-CoV-2, der das S-Protein kodiert. Die mRNA ist dabei von synthetischen Lipiden umhüllt und als Lipidnanopartikel verpackt, um die Stabilität des Impfstoffes zu verbessern und um vor allem die Aufnahme in die geimpften Muskelzellen und Zellen des Immunsystems zu ermöglichen.
Im Zytoplasma der geimpften Zellen läuft nun der Prozess der Translation ab: mit Hilfe der Ribosomen wird die Basensequenz der mRNA in die Aminosäuresequenz der Polypeptidkette, der Primärstruktur des späteren Proteins translatiert, d. h. übersetzt. In weiteren Prozessen wird die Polypeptidkette in die 3D-Struktur gefaltet und als fertiges Protein zur Zellmembran transportiert. Auf der Zelloberfläche präsentieren die Zellen nun das S-Protein von SARS-Cov-2 als Antigen und regen das Immunsystem zur Immunantwort an.
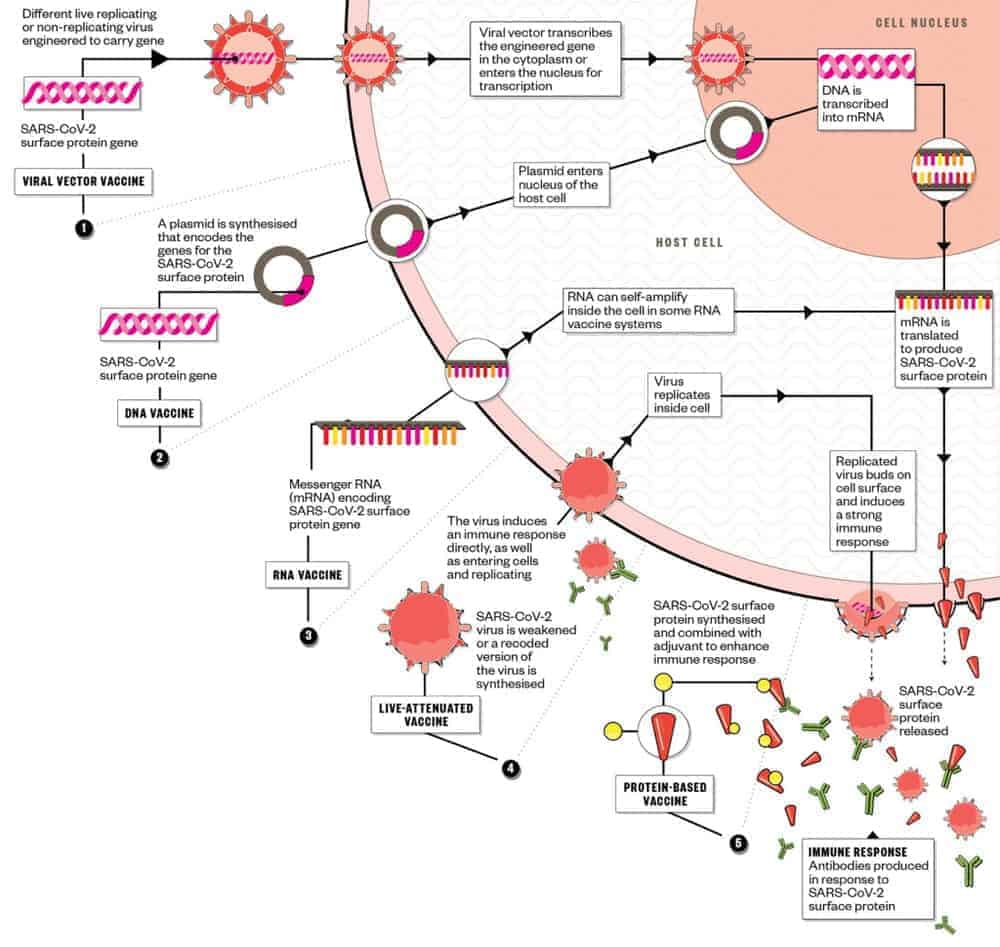
Abbildung. Die verschiedenen Arten von Impfungen. Die neuen mRNA-Impfstoffe fallen unter (3), die Vektor-Impfstoffe unter (1). Der Peptid-Impfstoff der Firma Novavax fällt unter (5). Quelle: https://clinicalaffairs.umn.edu/covid-19-updates/sars-cov-2-vaccine-development
Wie funktionieren Vektor-Impfstoffe?
Vektor-Impfstoffe gegen COVID-19 enthalten ein gentechnisch inaktiviertes und modifiziertes Adenovirus mit der genetischen Information für das S-Protein. Natürliche Adenoviren können Erkältung, Durchfall oder Bindehautentzündung verursachen.
Dagegen sind inaktivierte Vektorviren nicht vermehrungsfähig und können daher weder Symptome auslösen noch andere Menschen nach der Impfung anstecken. Vaxzevria® verwendet ein Adenovirus des Schimpansen, das Covid-19 Vaccine Janssen® dagegen ein humanes Adenovirus. Sputnik V® nutzt für die Erst- und Zweitimpfung zwei unterschiedliche humane Adenovirustypen.
Adenoviren haben – anders als Coronaviren – ein DNA-Genom. Daher wird für die Proteinbiosynthese des S-Proteins zunächst der Prozess der Transkription durchlaufen: im Zellkern wird die Basensequenz der doppelsträngigen DNA in die Basensequenz der einzelsträngigen RNA transkribiert, d. h. umgeschrieben. Die RNA gelangt als messenger RNA aus dem Zellkern in das Zytoplasma. Dort verlaufen die weiteren Prozesse nun analog zu den mRNA-Impfstoffen.
Können diese gentechnisch hergestellten Impfstoffe das menschliche Erbgut beeinflussen?
In Bezug auf die mRNA-Impfstoffe lässt sich die Frage nach der Integration in das menschliche Erbgut ganz klar mit Nein beantworten: die mRNA bleibt im Zytoplasma der Zelle wird nach der Translation sehr schnell wieder abgebaut.
Sie gelangt nicht in die Nähe der Chromosomen im Zellkern und kann in Form von einzelsträngiger RNA nicht in die doppelsträngige DNA eingebaut werden.
Wer sich nun fragt, was theoretisch passieren könnte, wenn die mRNA möglicherweise doch durch die Kernporen hindurch in den Zellkern gelangen könnte und dort auf eine reverse Transkriptase treffen könnte, erhält auch auf diese Bedenken eine eindeutige Antwort: aus molekulargenetischer Sicht ist es – nach allem, was wir wissen – ausgeschlossen, dass die RNA des Impfstoffs in DNA umgeschrieben wird.
Nach dem „zentralen Dogma der Molekulargenetik“ von Francis Crick, dem Entdecker der DNA, wird die genetische Information in der Regel nur in einer Richtung übertragen: von der DNA auf die RNA durch die Transkription und von der RNA auf das Protein durch die Translation.
Die reverse Transkription, d. h. die Umschreibung in umgekehrter Richtung von RNA in DNA, findet im menschlichen Körper nur in folgenden, sehr speziellen Ausnahmesituationen statt:
- bei der Reparatur der Telomere unserer Chromosomen durch das Enzym TERT (Telomerase-Reverse Transkriptase)
- bei der Transposition oder Replikation von bestimmten Retrotransposons
- bei einer Infektion mit Retroviren (z. B. HIV) oder Hepadnaviren (z. B. Hepatitis-B-Virus).
Man muss diese Prozesse nicht im Detail nachvollziehen, um den wesentlichen Punkt dabei zu verstehen: alle diese Prozesse benötigen eine komplementäre, d. h. genau passende Startsequenz, damit die beteiligten Enzyme an der RNA binden und die reverse Transkription starten können.
In der RNA-Sequenz der Impfstoffe gibt es aber keine zufällige Übereinstimmung mit diesen Startsequenzen. Es ist daher ausgeschlossen, dass Enzyme zur reversen Transkription an die Impfstoff-RNA binden können (2).
Was ist mit den Vektorimpfstoffen? Könnten diese unser Erbgut beeinflussen?
Bei den Vektorimpfstoffen lässt sich diese Frage dagegen nicht so eindeutig beantworten. Das Vektorvirus enthält die genetische Information für das S-Protein in Form von DNA und die DNA muss für die Transkription in den Zellkern gelangen, da nur dort die dazu nötigen Enzyme hergestellt werden.
Sowohl das Paul-Ehrlich-Institut (PEI) als auch das Robert-Koch-Institut (RKI) sehen „nach dem aktuellen Stand der Wissenschaft kein Risiko der Integration der Adenovirus-Vektor-DNA in das menschliche Genom“ aufgrund folgender Überlegungen (3,4):
- Die Transkription der Vektor-DNA findet zwar innerhalb des Zellkerns, aber außerhalb der menschlichen Chromosomen statt.
- Das Vektorvirus ist nicht vermehrungsfähig
- Selbst bei vermehrungsfähigen natürlichen Adenoviren ist die Integration in das menschliche Genom nicht erforderlich, da es sich bei den Adenoviren um nicht-integrierende Viren handelt.
- Der menschliche Körper hat regelmäßig Kontakt mit Adenoviren und bei einer natürlichen Infektion mit Adenoviren wurde bisher keine genetische Veränderung menschlicher Zellen beobachtet.
Nach Ansicht einzelner Experten kann jedoch nicht mit allerletzter Sicherheit ausgeschlossen werden, dass Virus-DNA im Rahmen der heterologen Rekombination in das menschliche Genom eingebaut werden könnte (5).
Die Frage geht also eher in die Richtung, welche Konsequenz eine Integration in das menschliche Genom hätte. Prof. Stefan Kochanek von der Abteilung für Gentherapie der Uni Ulm sieht in den Vektorimpfstoffen keine langfristige Gefahr, da „das Immunsystem eine Zelle, in die sich ein Adenovirus-Vektor ins Genom integriert hätte, sehr wahrscheinlich nach wenigen Wochen abtöten würde“.
Prof. Christian Münz vom Institut für experimentelle Immunologie der ETH Zürich sieht ebenfalls keine Gefahr der Entartung einer Zelle durch eine zufällige Integration an der falschen Stelle, da „es in der Regel mehrerer genetischer Veränderungen bedarf, damit ein Tumor entsteht“.
Enthalten die bisher zugelassenen COVID-19-Impfstoffe problematische Inhaltsstoffe wie Quecksilber, Aluminium oder Formaldehyd?
Die Inhaltsstoffe, die Du hier ansprichst, wurden oder werden bei einigen konventionellen Impfstoffen, aber nicht bei den COVID-19-Impfstoffen verwendet.
Quecksilber in Form von Thiomersal wird als Konservierungsstoff für Impfstoffe in Mehrdosenbehältern verwendet wie zuletzt bei dem „Schweinegrippen“-Impfstoff Pandemrix® (6).
Aluminiumhydroxid wird bei den meisten Toxoid- oder Totimpfstoffen als Adjuvans eingesetzt, um die Immunantwort zu verstärken.
Formaldehyd wird bei der konventionellen Impfstoffherstellung zur Abschwächung oder Inaktivierung von Viren eingesetzt und ist in den fertigen Präparaten möglicherweise noch in Spuren enthalten. Die Inaktivierung der Vektorviren erfolgt nicht mit Formaldehyd, sondern mit gentechnischen Verfahren.
Die Inhaltsstoffe von Impfstoffen, auch die der COVID-19-Impfstoffe, kannst Du in der Fachinformation einsehen. Nach deutschem Arzneimittelrecht (§11a AMG) müssen alle Inhaltsstoffe eines Medikaments in der Fachinformation aufgeführt sein. Auf europäischer Ebene entspricht die Fachinformation bei EU-weit zugelassenen Medikamenten der Zusammenfassung der Produktmerkmale (Summary of product characteristics).
Inhaltsstoffe von Comirnaty® (Biontech) (4):
- modifizierte mRNA
- synthetische Lipide: PEG-2000, ALC-0315 (ein künstliches Lipid), Colfoscerilstearat (Lipid aus Stearinsäure und Phosphorylcholin), Cholesterol
- Puffer: Kaliumchlorid, Kaliumdihydrogenphosphat, Natriumchlorid, Natriummonohydrogenphosphat
- Saccharose (Zucker)
Inhaltsstoffe des Covid-19 Vaccine Moderna® (4):
- modifizierte mRNA
- synthetische Lipide: PEG-2000, SM-102 (Lipid), Colfoscerilstearat, Cholesterin
- Puffer: TRIS (Puffer), Trometanolhydrochlorid, Essigsäure, Natriumacetat
- Sucrose (syn. Saccharose, Zucker)
Inhaltsstoffe von Vaxzevria® (AstraZeneca) (4):
- gentechnisch inaktiviertes und modizifiertes Schimpansen-Adenovirus
- Puffer: L-Histidin, L-Histidinhydrochlorid-Monohydrat, Natriumchlorid
- Polysorbat 80 (Emulgator)
- Sucrose (syn. Saccharose, Zucker)
- Ethanol (Alkohol)
- Natrium-EDTA (Konservierungsmittel)
Inhaltsstoffe des Covid-19 Vaccine Janssen® (4):
- gentechnisch inaktiviertes und modifiziertes humanes Adenovirus (HAdV26),
- Puffer: Natriumchlorid, Trinatriumcitrat-Dihydrat, Zitronensäure-Monohydrat, Salzsäure, Natriumhydroxid
- Polysorbat 80 (Emulgator)
- 2-Hydroxypropyl-b-Cyclodextrin (synthetisches Oligosaccharid)
- Ethanol (Alkohol)
Bei den Inhaltsstoffen handelt es sich um unbedenkliche Stoffe wie Puffer, Salze und Zucker zur Stabilisierung der Injektionslösung.
EDTA ist ein Komplexbilder, der als Konservierungsstoff, aber auch therapeutisch eingesetzt wird.
Aus allergologischer Sicht sind das PEG-2000 (Polyethylenglykol) und in deutlich geringerem Ausmaß das Polysorbat 80 als problematisch anzusehen, da diese Stoffe in vereinzelten Fällen zu schweren allergischen Sofortreaktionen (Anaphylaxien) führen können (3,4).
Sind diese Impfstoffe in Studien ausreichend getestet – oder handelt es sich eigentlich gerade um ein großes Experiment?
Ich kann gut nachvollziehen, dass zunächst eine gewisse Skepsis gegenüber den neuen Impfstoffen besteht. Zum einen gelang die Entwicklung der COVID-19-Impfstoffe so schnell wie noch nie – Prof. Ugur Sahin spricht von einer Entwicklung in „Lichtgeschwindigkeit“.
Zum anderen kommen mit den mRNA- und Vektor-Impfstoffen erstmals neue gentechnische Verfahren zum Einsatz. Die Entwicklung und die Zulassung der COVID-19-Impfstoffe haben aber alle regulären Prozesse durchlaufen, die dank der folgenden Faktoren beschleunigt werden konnten:
- Die Grundlagenforschung zu viralen Vektoren wird bereits seit den 70er Jahren betrieben und deren Anwendung in unterschiedlichen Bereichen wie der Gentherapie oder Krebstherapie wird seit den 90er Jahren erforscht.
- Zu den mRNA-basierten Therapien wird seit ca. 15 Jahren geforscht.
- Einige Impfstoffe mit viralen Vektoren sind bereits zugelassen: gegen Ebola, Dengue-Fieber und das Japanische-Enzephalitis-Virus (JEV). Viele weitere Vektorimpfstoffe sowie mRNA-Impfstoffe sind in der Entwicklung: u. a. gegen Influenza, HIV, Hepatitis C, Tollwut oder das Zika-Virus. Daher war bereits die „Plattform“ bekannt, die mit den gentechnischen Verfahren schnell an den neuen Erreger angepasst werden konnte. Denn aus der Entwicklung von Impfstoffen gegen SARS-CoV-1 und MERS-CoV, beides ebenfalls beta-Coronaviren, war bereits bekannt, dass sich das S-Protein als Antigen eignet.
- Die neuen Impfstoffe lassen den Körper das Antigen selbst herstellen. Dadurch entfällt die langwierige Kultivierung in Hühnereiern oder Zellkulturen zur Herstellung des Antigens.
- Für die Studien konnten wegen der pandemischen Bedeutung sehr schnell sehr viele Teilnehmer rekrutiert werden. Üblicherweise werden klinische Phase-III-Studien zu Impfstoffen mit ca. 3000 Teilnehmern durchgeführt. In den Zulassungsstudien der COVID-19-Impfstoffe wurden 10.000-40.000 Teilnehmer aufgenommen. Teilweise konnten die einzelnen Phasen der klinischen Studien überlappend durchgeführt werden.
- Im Prüfverfahren bei der EMA wurden beschleunigte Verfahren wie „rolling review“ und „bedingte Zulassung“ eingesetzt.
- Parallel zu den klinischen Studien und den Zulassungsverfahren wurden die Impfstoffe bereits vorproduziert, um nach Zulassung durch die EU-Kommission und Empfehlung auf nationaler Ebene durch die STIKO sofort ausgeliefert werden zu können.
Gibt es Unterschiede bei der Wirksamkeit der einzelnen Impfstoffe?
Die Wirksamkeit wird zunächst in den klinischen Phase-III-Studien untersucht, da für die Zulassung der Nachweis über eine ausreichende Wirksamkeit vorausgesetzt wird.
Sie bezieht sich auf die Reduktion der Wahrscheinlichkeit einer symptomatischen Erkrankung nach abgeschlossener Impfserie mit 2 Impfdosen.
- Die Wirksamkeit der mRNA-Impfstoffe liegt bei ca. 95 % (7,8). Stell dir vor, von 100 Personen erkranken 20 Placebo-Geimpfte an COVID-19. Von 100 Verum-Geimpften erkrankt dagegen nur eine Person.
- Vaxzevria® ist zu 82 % wirksam, wenn die 2. Impfung erst nach 12 Wochen gegeben wird (9). Von 100 Vaxzevria®-Geimpften würden in unserem Beispiel also nur 4 Personen erkranken.
- Nach Angaben des Herstellers variiert die Wirksamkeit von Covid-19 Vaccine Janssen® in den Ländern, in denen die Zulassungsstudien durchgeführt werden und wird als Gesamtergebnis mit 66% nach Impfung mit einer Einzeldosis angegeben (10). Von 100 Geimpften würden also 6 erkranken.
Alle Impfstoffe zeigten eine nahezu vergleichbar hohe Wirksamkeit bezogen auf einen schweren Krankheitsverlauf mit Behandlung im Krankenhaus sowie auf einen tödlichen Verlauf. Mit den Vektor-Impfstoffen wird diese Schutzwirkung bereits 3-4 Wochen nach der 1. Dosis, mit den mRNA-Impfstoffen 1-2 Wochen nach der 2. Dosis, d. h. bei derzeitigem Impfschema nach 7-8 Wochen erzielt (7-10).
Nach der Zulassung wird in den Beobachtungsstudien der Effekt der Impfung auf die Bevölkerung weiter untersucht und in den Kohorten Geimpfter gegenüber Nicht-Geimpften verglichen. Die bisherigen „Real-world“-Daten aus Schottland (11), England (12) und Israel (13) bestätigen die Ergebnisse zur Wirksamkeit der mRNA-Impfstoffe und Vaxzevria® aus den klinischen Studien.
| Comirnaty® | Moderna® | Vaxzevria® | Janssen® | |
| Hersteller | BioNTech / Pfizer | Moderna | AstraZeneca | Johnson & Johnson |
| Wirkprinzip | mRNA | mRNA | Vektor | Vektor |
| Zulassung bzw. STIKO-Empfehlung | Ab 16 Jahre | Ab 18 Jahre | Ab 60 Jahre | Ab 18 Jahre |
| Impfschema nach STIKO-Empfehlung | Zweite Dosis nach 6 Wochen | Zweite Dosis nach 6 Wochen | Zweite Dosis nach 12 Wochen | Einzeldosis |
| Studienkollektiv Phase-III Verum vs. Placebo | 18.508 vs. 18.435 (7) | 15.181 vs. 15.166 (8) | 5.807 vs. 5.829 (6) | 19.630 vs. 19.691 (10) |
| Wirksamkeit –symptomatische Erkrankung | 95% ab Tag 7 nach 2. Dosis (7) | 94% ab Tag 14 nach 2. Dosis (8) | 70% (bei Zweitimpfung nach 12 Wochen bis 82% (8)) | 66% (Südafrika 57%, Südamerika 66%, USA 72% (10)) |
| Wirksamkeit – Krankenhaus-behandlung | >95% ab Tag 7 nach 2. Dosis (7) | >95% ab Tag 14 nach 2. Dosis (8) | Nahezu 100% ab Tag 22 nach 1. Dosis (6) | Nahezu 100% ab Tag 28 (10) |
| Wirksamkeit – Tod | Annähernd 100% (7) | Annähernd 100% (8) | Annähernd 100% (6) | Annähernd 100% (10) |
| Wirksamkeit bei älteren Personen | Ab 65 Jahre 94 % ab Tag 7 nach 2. Dosis (7) | Ab 64 Jahre 86% ab Tag 14 nach 2. Dosis (8) | Ab 65 Jahre 90% Schutz vor schwerem Verlauf ab Tag 22 nach 1. Dosis (11) | Ab 60 Jahre vermindert, aber Schutz vor schwerem Verlauf (10) |
Schützen die Impfstoffe auch vor den neuen Covid-Mutanten?
Das SARS-CoV-2 mutiert wie andere Coronaviren ständig, aber eine einzelne Mutation hat keinen großen Einfluss auf die Wirksamkeit der COVID-19-Impfstoffe, da sie eine polyklonale Immunantwort hervorrufen (3).
Das bedeutet, dass viele unterschiedliche Antikörper und T-Zellen gegen unterschiedliche Bereiche des S-Proteins (Epitope), gebildet werden. Da alle COVID-19-Impfstoffe auf dem S-Protein als Antigen basieren, geht das RKI prinzipiell von einer ähnlichen Auswirkung einer Mutation auf die Wirksamkeit der Impfstoffe aus.
Bei den aktuellen VOC (den Variants of Concern) gibt es teilweise Einschränkungen der Wirksamkeit. Die Hersteller entwickeln daher bereits Update-Impfstoffe, die an die aktuellen VOC angepasst sind. Sie rechnen mit einer Zulassung ab Herbst.
Was bedeutet das für Mutanten wie z. B. B.1.1.7 oder P.1 aus Brasilien?
Die Variante B.1.1.7 hat sich im Herbst 2020 zunächst in Großbritannien ausgebreitet und ist inzwischen die in Europa und Nordamerika vorherrschende Virusvariante.
Sie weist 23 Mutationen auf, davon befinden sich 8 im Bereich des S-Protein. Trotzdem gilt inzwischen als gesichert, dass die Impfstoffe bei der „normalen“ Variante B.1.1.7, d. h. ohne zusätzliche Escape-Mutation wirksam sind (6).
Die aktuell noch seltene Sonderform B.1.1.7 E484K hat eine zusätzliche Mutation im S-Protein: an Position 484 ist die Aminosäure Glutaminsäure gegen Lycin ausgetauscht. Diese Position liegt im Bereich der Bindungsdomäne, mit der das Virus an den Rezeptor der Wirtszelle bindet.
Sie wird auch als Escape-Mutation bezeichnet, weil sie den neutralisierenden Antikörpern teilweise entkommt. Die Mutation beeinflusst nicht nur die Passform des S-Proteins, sondern erhöht die Bindungsaffinität mit dem Rezeptor so stark, dass das Virus trotz vorhandener Antikörper an den Rezeptor binden und in die Wirtszelle eindringen kann.
Daher breitet sich die Escape-Varianten in den Populationen aus, in denen zu einem hohen Anteil eine Teilimmunität nach einer durchgemachten Infektion besteht.
Prof. Christian Drosten hat im NDR-Podcast vom 30.03.2021 die aktuelle Datenlage zur Wirksamkeit der Impfstoffe bei Varianten mit der Escape-Mutation folgendermaßen zusammengefasst: Bei Neutralisationsversuchen im Labor hat sich gezeigt, dass die neutralisierende Wirkung der Antikörper durch den Immun-Escape vor allem nach Infektion, aber auch nach Impfung abgeschwächt ist.
Die Antikörper als Teil der humoralen Antwort schützen vor der Ansteckung und vor einem leichten Krankheitsverlauf. Dagegen schützt die zelluläre Immunantwort vor einem schweren Krankheitsverlauf.
Eine aktuelle Studie zeige, dass die zelluläre Immunität durch den Immunescape nicht wesentlich beeinträchtigt ist. Prof. Drosten geht daher davon aus, dass die Impfstoffe trotz der Escape-Mutation eine deutliche Schutzwirkung in Bezug auf einen schweren Krankheitsverlauf haben.
B.1.351 ist die dominierende Variante in Südafrika. Sie ist in Europa nur selten nachweisbar.
Die Variante P.1 breitet sich derzeit in Brasilien aus und wird in Europa nur vereinzelt nachgewiesen.
Beide VOC haben u. a. die E484K-Mutation und zeigen eine abgeschwächte Wirkung der neutralisierenden Antikörper, bei B.1.351 schwächer als bei P.1 (6). Die Phase-III-Studie zum Covid-19 Vaccine Janssen® ist auf drei Studienarme in Südafrika, Südamerika und den USA aufgeteilt (10).
Zum Zeitpunkt der Durchführung waren die VOC B.1.351 und P.1 bereits die vorherrschenden Varianten in Südafrika und Südamerika.
Dadurch erklärt sich – zumindest teilweise – die unterschiedliche Wirksamkeit in den verschiedenen Studienarmen: in Südafrika 57%, in Südamerika 66% und in den USA 72%.
Die Zwischenauswertung der Studie belegt aber auch die hohe Schutzwirkung in Bezug auf einen schweren Krankheitsverlauf in allen drei Regionen.
Wie lange hält die Schutzwirkung der Impfungen an?
Die Studien, die das untersuchen, laufen noch. Aus einer Pressemitteilung von BioNTech/Pfizer ist bekannt, dass die Wirksamkeit von Comirnaty® 6 Monate nach der Zweitimpfung 91% beträgt (14).
Welche Nebenwirkungen können im Zusammenhang mit einer COVID-19-Impfung auftreten?
Bei den Nebenwirkungen muss man zwischen der normalen Impfreaktion, Impfkomplikationen und Langzeitfolgen differenzieren.
Die hohe Wirksamkeit der COVID-19-Impfstoffe geht mit einer vergleichsweise starken, aber unbedenklichen Impfreaktion einher.
Daher kommt es häufiger zu stärkeren Beschwerden. Vektor-Impfstoffe führen häufiger nach der 1. Impfung, mRNA-Impfstoffe dagegen häufiger nach der 2. Impfung zu Beschwerden.
Jüngere Impflinge zeigen häufiger als ältere eine Impfreaktion.
Das Ausmaß der Impfreaktion korreliert aber nicht mit der Immunantwort und der zu erwartenden Schutzwirkung. Die Impfreaktion setzt nach 1-2 Tagen ein und kann 1-2 Tage anhalten. Die Beschwerden äußern sich lokal mit Schmerzen im Oberarmmuskel oder systemisch mit Kopfschmerzen, Müdigkeit, Muskelschmerzen, Fieber und Schüttelfrost (3). Ein Drittel der Vaxzevria®-Geimpften und 20% der Comirnaty®-Geimpften sind beschwerdefrei (3).
Impfkomplikationen gehen über das Maß einer normalen Impfreaktion hinaus. In seltenen Fällen kann es in Folge einer Reaktion des vegetativen Nervensystems zu einer vorübergehenden Ohnmacht (vasovagale Synkope) kommen. Daher werden in den Impfzentren alle Geimpften für 15 Minuten nachbeobachtet.
Anaphylaxie
In vereinzelten Fällen kann eine allergische Sofortreaktion mit Kreislaufschock (Anaphylaxie) auftreten. Das Paul-Ehrlich-Institut berichtet im Sicherheitsreport vom 09.04.2021 von bisher 87 Fällen nach ca. 10,7 Millionen Impfungen mit Comirnaty®, 2 Fällen nach ca. 700.000 Impfungen mit dem Covid-19 Vaccine Moderna® sowie 14 Fällen nach 2,9 Millionen Impfungen mit Vaxzevria®. Bei erhöhtem Risiko einer allergischen Sofortreaktion wird die Nachbeobachtung im Impfzentrum auf 30 Minuten verlängert.
Gesichtslähmung
Bereits in den Zulassungsstudien der mRNA-Impfstoffe wurden vereinzelte Fälle einer Gesichtslähmung (idiopathische Fazialisparese, Bell-Parese) berichtet, sodass diese mögliche Komplikation im Aufklärungsmerkblatt aufgeführt ist (3). Bei der überwiegenden Zahl der Betroffenen bildete sich die Gesichtslähmung innerhalb von Wochen zurück.
Das PEI berichtet im Sicherheitsreport vom 04.03.2021 über 14 Fälle einer Fazialisparese nach ca. 6 Millionen Impfungen mit Comirnaty® und 360.000 Impfungen mit dem Covid-19 Vaccine Moderna®, in denen ein ursächlicher Zusammenhang mit der Impfung nicht ausgeschlossen werden kann, aber als fraglich angesehen wird, da die Anzahl der Fälle die Hintergrundinzidenz nicht übertraf.
Atypische Thrombosen
Wegen der äußerst geringen Fallzahlen zeigte sich erst nach der Zulassung im Rahmen der sog. Pharmakovigilanz eine Häufung von ungewöhnlichen Thrombosen wie z. B. Sinusvenenthrombosen in Zusammenhang mit Vaxzevria®.
Stand 02.04.2021 waren 42 Verdachtsfälle nach 2,9 Millionen Impfungen mit Vaxzevria® bekannt (4). Prof. Greinacher et al. von der Abteilung für Transfusionsmedizin der Uniklinik Greifswald entdeckten den mutmaßlichen und plausiblen Pathomechanismus dieser Komplikation mit dem neuen Namen VITT (Vaccine-induced immune thrombotic thrombocytopenia): im Rahmen der Immunstimulation werden Autoantikörper gegen den Plättchenfaktor 4 (PF4) gebildet.
Diese Autoantikörper bewirken eine Aktivierung der Blutplättchen und in der Folge die Thrombose, den Abfall der Blutplättchen und ggfs. Blutungen (15). Wegen der Seltenheit dieser Komplikation werden noch weitere beteiligte Faktoren vermutet. Zudem ergeben sich aus diesen Erkenntnissen Möglichkeiten der Diagnostik und Therapie.
Vorbeugende Maßnahmen sind noch nicht etabliert. Es gilt als gesichert, dass diese untypischen Thrombosen nach Impfung – im Gegensatz zu den normalen Thrombosen – eine immunologische Ursache haben.
Daher haben Patientinnen und Patienten mit einer „normalen“ Thrombose in der Vorgeschichte und / oder einer bekannten Thrombophilie (z. B. Faktor-V-Leiden-Mutation, von-Willebrand-Syndrom) kein erhöhtes Risiko für diese atypischen Thrombosen.
Die EMA hält es für unwahrscheinlich, dass die anderen Vektor-Impfstoffe ebenfalls zu dieser Komplikation führen werden, da die Autoantikörper am wahrscheinlichsten durch den Vektor induziert werden und sich die Oberfläche des Schimpansen-Adenovirus in Vaxzevria® von den humanen Adenoviren der anderen Vektor-Impfstoffe unterscheidet. Zudem wird Sputnik V® seit Ende 2020 in vielen Ländern bereits verimpft und bisher wurden keine Fälle gemeldet.
Auf der anderen Seite wurden bereits gehäuft Bedenken geäußert, dass es nicht der Vektor ist, der die Thrombosen induziere kann, sondern das Spike-Protein selbst. Daher könnten diese Komplikationen bei allen Impfungen auftreten – hier wird die Zukunft zeigen, ob die EMA mit ihren Aussagen recht behält, oder nicht.
Sind Langzeitfolgen wie Autoimmunerkrankungen oder Krebs möglich?
Autoimmun- und Krebserkrankungen haben nicht nur eine einzelne Krankheitsursache. Sie werden multifaktoriell verursacht und entstehen aus einer komplexen Wechselwirkung von genetischer Veranlagung, Umwelteinflüssen und Lebensstil.
Daher wäre es sehr unwahrscheinlich, dass ein einzelner Umweltfaktor wie eine Impfung Krebs oder eine Autoimmunerkrankung verursachen würde. Bisher haben sich weder in den präklinischen und klinischen Studien noch aus der Anwendung Hinweise darauf ergeben (3,4). Allerdings ist die bisherige Nachbeobachtungszeit der klinischen Studien noch nicht ausreichend, um gesicherte Aussagen zu Langzeitfolgen machen zu können.
Lass uns noch die häufigsten Fake News in Zusammenhang mit den COVID-19 Impfungen besprechen. Stimmt es, dass die Impfung unfruchtbar macht?
Nein, das ist nicht der Fall!
Diese Fehlinformation beruht auf dem „wahren Kern“, dass die Aminosäuresequenz des S-Proteins und des plazentaren Proteins Syncytin-1 über 5 Positionen hinweg beinahe identisch ist.
Eine Kreuzreaktion der Antikörper mit Syncytin-1 ist aber trotzdem nicht möglich: Zum einen ist diese zufällige Übereinstimmung viel zu kurz. Zum anderen ist die betreffende Sequenz von Syncytin-1 Teil der Transmembrandomäne und wäre daher zwischen den beiden Lipidschichten der Zellmembran gar nicht erreichbar für kreuzreagierende Antikörper (16). Im Labor hat sich gezeigt, dass das Rekonvalenz-Serum (von Genesenen) nicht mit Syncytin-1 reagiert (6).
Außerdem: Wenn die Impfung unfruchtbar machen würde, müsste COVID-19 auch unfruchtbar machen. Das ist aber weltweit nicht beobachtet worden. Frauen mit Kinderwunsch wird die Impfung von der STIKO, der DGGG (Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (17)) und anderen Fachgesellschaften ausdrücklich empfohlen.
Stimmt es, dass die COVID-19-Impfungen Lungenentzündungen verursachen?
Mit dieser Frage sprichst Du das Phänomen der infektionsverstärkenden Antikörper an (ADE, Antibody-dependent enhancement), das es tatsächlich gibt, beispielsweise beim Dengue-Fieber.
Bei der Erstinfektion werden Antikörper gebildet, welche bei der Zweitinfektion an das Virus binden und – anstatt das Virus zu neutralisieren – die Aufnahme in bestimmte Immunzellen ermöglichen. Dadurch kommt es bei der Re-Infektion zu einer Verstärkung der Infektion.
Da sich bei der Entwicklung von Impfstoffen gegen SARS-CoV-1 und MERS-CoV Hinweise auf Probleme mit ADE ergeben haben, wurden diese Erkenntnisse bei der Entwicklung der COVID-19-Impfstoffe mit einbezogen. Das S-Protein wurde so optimiert, dass es der Bildung von ADE entgegenwirkt. Bisher gibt es weder in Zusammenhang mit einer natürlichen COVID-19-Erkrankung noch mit einer COVID-19-Impfung Hinweise auf ADE (4).
Stimmt es, dass die COVID-19-Impfstoffe Mikro- oder Nanochips enthalten?
Nein, auf keinen Fall!
Offenbar wurden diese Mikrochips mit sog. Quantum dot tattoos verwechselt, die in einem Projekt der Gates Foundation verwendet worden sind.
Hintergrund dieses Projekts war die in Entwicklungsländern erschwerte Dokumentation darüber, wer wann gegen was geimpft wurde.
Mit den Quantum dot tattoos wurde zusammen mit dem Impfstoff ein nicht sichtbarer, fluoreszierender, ca. 5 Jahre haltbarer Farbstoff injiziert. Aus nächster Nähe konnten damit Informationen zur Impfung ausgelesen werden (18).
Die aktuell kleinsten implantierbaren Chips mit RFID- oder NFC-Technologie sind immerhin 2×12 mm groß und würden gar nicht durch die zur Impfung verwendete Kanüle passen.
Wer sollte sich nicht impfen lassen oder besondere Vorsichtsmaßnahmen treffen?
Aktuell gilt nur für Kinder und Jugendliche bis 15 Jahre, dass eine Impfung grundsätzlich nicht möglich ist.
Comirnaty® ist aktuell erst ab 16 Jahren zugelassen. Bei den Herstellern laufen aber schon Studien an Jugendlichen, Kindern und sogar Babys ab 6 Monaten.
BioNTech/Pfizer gab in einer Pressemitteilung bekannt, dass in der Phase-III-Studie mit 2000 Jugendlichen zwischen 12 und 15 Jahren in der Gruppe der Geimpften kein Teilnehmer erkrankte und somit auch in dieser Altersgruppe eine hohe Wirksamkeit besteht (19). Es besteht die Aussicht auf eine Zulassung im Herbst, z. B. für chronisch kranke Kinder.
In folgenden Konstellationen ist eine Impfung nach Rücksprache mit der Ärztin oder dem Arzt bzw. unter Beachtung besonderer Vorsichtsmaßnahmen möglich:
- Die EMA bewertet den kausalen Zusammenhang zwischen den untypischen Thrombosen in Kombination mit Thrombozytopie und der Impfung mit Vaxzevria® noch nicht als gesichert, aber „möglich“. Der Impfstoff ist daher weiterhin ab 18 Jahren zugelassen. Auf nationaler Ebene empfiehlt die STIKO die Impfung mit Vaxzevria® (AstraZeneca) für Personen unter 60 Jahre nicht mehr regulär. Der Einsatz dieses Impfstoffs bleibt aber „nach ärztlichem Ermessen und bei individueller Risikoakzeptanz nach sorgfältiger Aufklärung möglich“ (3).
- Für Personen unter 60 Jahre, die bereits eine Erstimpfung mit Vaxzevria® erhalten haben empfiehlt die STIKO vorläufig die Zweitimpfung mit einem mRNA-Impfstoff. Aktuell laufen „Mix-and-Match“-Studien zu Sicherheit und Wirksamkeit bei sog. heterologem Impfschema mit unterschiedlichen Impfstoffen. Die Ergebnisse werden für Ende April / Anfang Mai erwartet.
- Für Schwangere spricht die STIKO aktuell (noch) keine generelle Empfehlung aus, da die aktuell vorhandene Datenlage zur Anwendung in der Schwangerschaft noch nicht ausreichend ist. Daher werden zunächst Kontaktpersonen priorisiert geimpft. Nach Einschätzung der STIKO und der DGGG (17) können Schwangere im Einzelfall und nach Besprechung mit dem Arzt eine Impfung erhalten. Aktuell laufen Phase-III-Studien an Schwangeren zu Sicherheit und Wirksamkeit der Impfung mit Comirnaty® und dem Covid-19 Vaccine Janssen®.
- Frauen in der Stillzeit empfiehlt die DGGG die Impfung zum Zeitpunkt, an dem sie nach Priorisierung regulär vorgesehen ist (20).
- Bei akuten fieberhaften Infektionen (mit Fieber über 38,5 °C) soll nicht geimpft werden (3).
- Zu anderen geplanten Impfungen soll ein Abstand von 14 Tagen eingehalten werden (3).
- Bei einer nachgewiesenen COVID-19-Infektion empfiehlt die STIKO 6 Monate später eine einmalige Boost-Impfung. Nach Ansicht des RKI ist es nicht notwendig, vor einer geplanten Impfung einen Antikörper-Test durchzuführen, um eine unbemerkte Infektion auszuschließen. Ich persönlich habe vor meiner Impfung einen Test auf SARS-CoV-2-IgG durchführen lassen, um das Risiko der Impfung nicht unnötigerweise einzugehen.
- Personen mit einer Immunschwäche in Folge von immunsuppressiven Therapien, Krebstherapien oder chronischen Erkrankungen wird wegen des höheren Risikos für einen schweren Krankheitsverlauf eine Impfung empfohlen (3, 21, 22). Möglicherweise ist unter diesen Umständen die Wirksamkeit vermindert. Bei Einnahme von Immunsuppressiva empfiehlt es sich, mit der behandelnden Ärztin oder dem Arzt eine Anpassung der Medikamente bzw. ein günstiges Zeitintervall für die Impfung zu besprechen. Weitere Informationen finden Betroffene auch bei den entsprechenden Fachgesellschaften.
- Personen mit einer Autoimmunerkrankung ohne immunsuppressive Therapie waren in den Zulassungsstudien eingeschlossen. Dabei zeigte sich, dass durch die Impfung kein Schub der Grunderkrankung zu erwarten ist.
- Personen mit einer Anaphylaxie unklarer Ursache in der Vorgeschichte oder mit einer bekannten Allergie gegen einen der Inhaltsstoffe, insbesondere PEG, wird vor der Impfung mit einem mRNA-Impfstoff die Vorstellung in einem allergologischen Zentrum empfohlen (3, 23). PEG sind z. B. in Kosmetika und in Medikamenten wie Abführmitteln oder Darmspüllösungen enthalten. Bei folgenden Allergien ist die Impfung aus allergologischer Sicht unbedenklich: allergische Rhinokonjunktivitis (Heuschnupfen oder Hausstaubmilbenallergie), Allergisches Asthma, Insektengiftallergie (auch bei Anaphylaxie), Nahrungsmittelallergie, allergisches Kontaktekzem, Urtikaria, Neurodermitis, Arzneimittelexanthem (3, 23).
- Bei Personen mit Hämophilie oder Einnahme bestimmter blutverdünnender Medikamente (direkte und indirekte orale Antikoagulanzien) wird die geimpfte Stelle zur Unterstützung der Blutgerinnung für 2 Minuten komprimiert und der Impfling wird für 30 Minuten auf eine Nachblutung nachbeobachtet.
Muss ich mich impfen lassen?
Nein, es besteht keine Impfpflicht.
Kann ich mich impfen lassen?
Nach der Impfverordnung des BMG (Bundesgesundheitsministeriums) werden drei Priorisierungsgrupen mit erhöhter Priorität gegenüber der allgemeinen Bevölkerung (Prioritätsgrad 4) definiert. Für die Organisation und Durchführung der Impfkampagne sind die Länder zuständig. In Hamburg und Schleswig-Holstein werden z. Zt. die Priorisierungsgruppen 1 und 2 geimpft.
Auch die Hausärzte, die nun auch mit dem Impfen begonnen haben, sind an die in der Impfverordnung definierte Priorisierung gebunden.
Soll ich mich impfen lassen?
Die Antwort ist komplex, da viele verschiede Aspekte eine Rolle spielen. Man muss die Risiken der Impfung gegenüber den Risiken der Erkrankung und dem Nutzen der Impfung abwägen. Am Ende muss jeder selbst eine Antwort für sich finden.
In diesem Interview liegt der thematische Schwerpunkt auf den Impfungen und deren möglichen Risiken. Daher überwiegen nach dem Lesen möglicherweise die Bedenken vor einer COVID-19-Impfung. Um eine ausgewogene Entscheidung für oder gegen eine Impfung zu treffen, muss man sich aber auch mit den Risiken einer COVID-19-Infektion auseinandersetzen.
Aktuell befinden wir uns in der 3. Welle in einer Situation mit ansteigenden Fallzahlen in der jüngeren Bevölkerung und einer flächendeckenden Ausbreitung der ansteckenderen und auch gefährlicheren Variante B.1.1.7 (3).
Die Wahrscheinlichkeit einer Ansteckung ist hoch und kumuliert mit jedem Tag, den die Pandemie noch weiter anhält.
Die Infektion mit SARS-CoV-2 kann unabhängig von der Schwere des Krankheitsverlaufs auch zu Long-COVID und anderen neurologischen und kardiovaskulären Komplikationen führen. Nicht nur die Impfungen sind neu – auch das Virus ist neu und nach einem Jahr der Pandemie können wir möglicherweise noch nicht alle Langzeitkomplikationen der Infektion erfassen.
Eine Ansteckung ist aber nicht gleichzusetzen mit einer Infektion. Die krankmachende Wirkung (Pathogenität) eines Erregers wird nicht nur von dessen “Gefährlichkeit” (Virulenz), sondern auch von der Wechselwirkung mit dem Immunsystem beeinflusst. Das bedeutet: je robuster mein Immunsystem ist, desto weniger wahrscheinlich werde ich nach einer Ansteckung auch tatsächlich krank – und desto geringer ist der Nutzen einer Impfung.
Ältere oder vorerkrankte Personen mit einem hohen Risiko für einen schweren Krankheitsverlauf haben einen höheren Nutzen der Impfung. Daher wird ihnen die Entscheidung zur Impfung leichter fallen als jungen und gesunden Personen. Aber auch jemand, der aus Sicht der klassischen Medizin als “jung und gesund” gilt, kann in Folge von Lebensstilfaktoren unter Umständen ein schwaches Immunsystem haben.
Auf der anderen Seite beeinflusst das Immunsystem wiederum die Risiken der Impfung. Ein starkes Immunsystem macht – neben weiteren Faktoren – weniger empfänglich für Allergien, Kreuzreaktionen und eventuelle Langzeitkomplikationen.
Folgende Fragen können dabei helfen, sich ein Bild über die eigene Situation zu machen:
- Wie viele Kontakte habe ich jeden Tag?
- Trage ich bei diesen Kontakten eine Maske und halte ich den Abstand ein?
- Kann bzw. möchte ich die weitere Reduktion dieser Kontakte selbst beeinflussen?
- Welche Kontakte haben weitere Familien- oder Haushaltsangehörige?
- Wie schätze ich im Fall einer Ansteckung das Risiko für einen schweren Krankheitsverlauf aufgrund meines Alters und meines Gesundheitszustand ein?
- Wie schätze ich im Fall einer Ansteckung das Risiko für ein Long-COVID ein?
- Habe ich Kontaktpersonen mit einem erhöhten Risiko für einen schweren Krankheitsverlauf mit COVID-19?
- Wie schätze ich die Risiken in Zusammenhang mit einer Impfung für mich ein?
- Wie schätze ich mein Immunsystem ein?
Dazu können Online-Tools helfen, das eigene Risiko einschätzen. Einfache Tools wie covid-o-mat.de berechnen die Wahrscheinlichkeit, bei einem Ereignis auf eine infizierte Kontaktperson zu treffen.
Komplexere Tools wie der COVID-Rechner von FOCUS Online oder der Covid 19 Aerosol Transmission Risk Calculator des Max-Planck-Instituts berechnen das Risiko der eigenen Ansteckung bei einem Ereignis.
Auch, wenn die mathematischen Modelle eine genaue Zahl errechnen, ist zu berücksichtigen, dass das Ergebnis nur einen Eindruck vermitteln kann. Die Angaben zu den Impfkomplikationen sind dadurch verzerrt, dass zunächst in zwei unterschiedlichen Populationen geimpft wurde – Comirnaty® bei den über 80-jährigen und Vaxzevria® bei jüngeren Personen.
Exakte Berechnungen zum Long- COVID sind noch nicht möglich, weil dieses Krankheitsbild bisher noch nicht einheitlich definiert werden kann.
Wenn man die Frage nach dem Nutzen der Impfung aus gesellschaftlicher Sicht betrachtet, ist ganz klar, dass wir mit der Impfung das wirksamste Mittel zur Bewältigung der Pandemie haben. Nicht das einzige Mittel, aber das wirksamste.
Es gilt inzwischen als gesichert, dass die Übertragung von SARS-CoV-2 durch die Impfung deutlich reduziert wird. Das bedeutet, dass mit jeder geimpften Person eine Infektionskette unterbrochen werden kann.
Durch den Aufbau der Herdenimmunität werden auch diejenigen geschützt, die nicht geimpft werden können. Dazu wirkt die Impfung der Selektion und Verbreitung von Escape-Varianten entgegen, da die Immunantwort auf eine vollständige Impfserie höher ist als nach einer durchgemachten Infektion (3).
Wie kann ich mich auf die Impfung vorbereiten, um das Ansprechen zu erhöhen und Nebenwirkungen erträglicher zu machen?
Ein starkes Immunsystem ist wichtig für die Immunantwort auf die Impfung und macht weniger empfänglich für Komplikationen. Daher ist es von Vorteil, wenn man sich schon einige Zeit vor der Impfung vorbereitet.
Empfehlungen von Martin umfassen kalte Duschen, eine gesunde Ernährung und eine ausreichende Versorgung mit wichtigen Nähr- und Vitalstoffen (v.a. Vitamin A, Vitamin C, Vitamin D, Zink, Omega 3-Fettsäuren). Auch Reishi und N-Acetyl-Cystein sind gute Wege zur Immunstärkung und Vorbereitung.
Im Impfzentrum empfehle ich den Impflingen: leichte Bewegung an der frischen Luft, gesund kochen, viel schlafen, auf Alkohol und Zigaretten verzichten.
Medikamente sollten nicht eingenommen werden, um Beschwerden durch die Impfreaktion vorzubeugen. Paracetamol wirkt fiebersenkend und schmerzlindernd, Ibuprofen wirkt zusätzlich auch entzündungshemmend. Die Antikörperproduktion kann dadurch beeinträchtigt werden.
So lange die Beschwerden durch die Impfreaktion noch erträglich sind, sollte man zunächst abwarten. Wenn man aber doch unter starken Kopfschmerzen oder hohem Fieber leidet, zeigt das, dass die Impfreaktion bereits voll in Gang ist. Die Einnahme von Paracetamol hätte dann keine nachteiligen Auswirkungen mehr.
Ibuprofen sollte nur eingenommen werden, falls Einwände gegen Paracetamol bestehen.
Wo kann ich weitere Informationen finden?
Zur Übersicht sind die relevanten und aktuell verfügbaren Informationen in den Faktenblättern (24) und den Aufklärungsmerkblättern (25) des RKI kurz zusammengefasst. Diese findest Du im Quellenverzeichnis.
Zu detaillierteren Fragen sind in den FAQ zur COVID-19-Impfung des RKI (26), des Paul-Ehrlich-Institut (PEI) (27) und der Bundeszentrale für gesundheitliche Aufklärung (28) jeweils aktuelle und wissenschaftlich fundierte Antworten zu finden.
Das PEI veröffentlicht alle 1-2 Wochen einen Sicherheitsreport (29), in dem die Sicherheit der Impfstoffe in Hinblick auf die gemeldeten Nebenwirkungen und Komplikationen fortlaufend bewertet wird.
Die Produktinformationen der einzelnen Impfstoffe können ebenfalls auf der Seite des PEI eingesehen werden.
Frauen mit Kinderwunsch und schwangere oder stillende Frauen finden in den Stellungnahmen der DGGG (17, 20) die für sie relevanten Informationen zur Impfung. Zu speziellen Fragestellungen in Zusammenhang mit chronischen Erkrankungen stellen die entsprechenden Fachgesellschaften Informationen zur Verfügung.
Liebe Elke, vielen Dank für das ausführliche Interview und die Mühe!
- Lenzen-Schulte M. Long COVID: Der lange Schatten von COVID-19. www.aerzteblatt.de 2020.
- Nirenberg E. No, Really, mRNA Vaccines Are Not Going To Affect Your DNA. www.deplatformdesease.com 2021.
- www.rki.de (abgerufen am 12.04.2021)
- www.pei.de (abgerufen am 12.04.2021)
- Jötten F. Können Vektorimpfstoffe das Erbgut verändern? www.pharmazeutische-Zeitung.de 2021.
- www.gelbe-liste.de (abgerufen am 09.04.2021)
- Rubin EJ, Longo DL. SARS-CoV-2 Vaccination – An Ounce (Actually, Much Less) of Prevention. N Engl J Med. 2020 Dec 31;383(27):2677-2678.
- Baden LR et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. N Engl J Med. 2021 Feb 4;384(5):403-416.
- Voysey M et al. Single-dose administration and the influence of the timing of the booster dose on immunogenicity and efficacy of ChAdOx1 nCoV-19 (AZD1222) vaccine: a pooled analysis of four randomised trials. Lancet. 2021 Mar 6;397(10277):881-891.
- Johnson & Johnson Announces Single-Shot Janssen COVID-19 Vaccine Candicate Met Primary Endpoints in Interim Analysis of its Phase 3 ENSEMBLE Trial. www.jnj.com 2021.
- Vasileiou E et al. Effectiveness of first dose of COVID-19 vaccines against hospital admissions in Scotland: national prospective cohort study of 5.4 million people www.medrxiv.org 2021.
- Lopes Bernal J et al. Early effectiveness of COVID-19 vaccination with BNT162b2 mRNA vaccine and ChAdOx1 adenovirus vector vaccine on symptomatic disease, hospitalisations and mortality in older adults in England www.medrxiv.org 2021.
- Dagan N et al. mRNA Covid-19 Vaccine in a Nationwide Mass Vaccination Setting. N Engl J Med. 2021 Feb 24:NEJMoa2101765
- Biontech: Gute Schutzwirkung über mindestens 6 Monate, bisher kein Einbruch durch B.1.351. www.aerzteblatt.de 2021.
- Greinacher A et al. Thrombotic Thrombocytopenia after ChAdOx1 nCov-19 Vaccination. N Engl J Med. 2021 Apr 9. doi: 10.1056/NEJMoa2104840. Epub ahead of print. PMID: 33835769.
- www.uni-jena.de/210127_Impfmythen
- https://www.dggg.de/presse-news/pressemitteilungen/mitteilung/covid-19-schutzimpfung-von-schwangeren-und-frauen-mit-kinderwunsch-1285/
- Nowotny R. Gates: Mikrochip-Implantate gegen Coronavirus? – Der Faktencheck. www.mimikama.at 2020.
- https://investors.biontech.de/de/node/9576/pdf
- https://www.dggg.de/fileadmin/documents/pressemitteilungen/2020/Hinweise_fuer_Stillende_zur_COVID-19-Impfung.pdf
- Geisen UM et al. Immunogenicity and safety of anti-SARS-CoV-2 mRNA vaccines in patients with chronic inflammatory conditions and immunosuppressive therapy in a monocentric cohort. Ann Rheum Dis. 2021 Mar 24:annrheumdis-2021-220272.
- https://www.dggg.de/leitlinien-stellungnahmen/stellungnahmen/covid-19-schutzimpfung-bei-patientinnen-mit-aktiver-krebserkrankung-1292/
- Worm M et al. Anaphylaxie-Risiko bei der Covid-19-Impfung: Empfehlungen für das praktische Management. MMW Fortschr Med 2021.
- https://www.rki.de/DE/Content/Infekt/Impfen/Materialien/Faktenblaetter/Faktenblaetter_inhalt.html
- https://www.rki.de/DE/Content/Infekt/Impfen/ImpfungenAZ/COVID-19/Aufklaerungsbogen-Tab.html
- https://www.rki.de/SharedDocs/FAQ/COVID-Impfen/gesamt.html
- https://www.pei.de/DE/service/faq/coronavirus/faq-coronavirus-node.html
- https://www.infektionsschutz.de/coronavirus/schutzimpfung/fragen-und-antworten.html
- https://www.pei.de/DE/newsroom/dossier/coronavirus/coronavirus-inhalt.html?cms_pos=5
Dr. med. Elke Lenhart studierte Humanmedizin an der RWTH Aachen und war während des Studiums als medizinische Doktorandin am Institut für Humangenetik im Forschungsprojekt „Molekulargenetische Grundlagen der Präeklampsie“ tätig. Nach ihrer Promotion absolvierte sie ihre Facharztweiterbildung in Gynäkologie und Geburtshilfe in der Schweiz und in der Asklepios Klinik Barmbek in Hamburg.
Heute arbeitet sie hauptberuflich als ärztliche Gutachterin und Beraterin für sozialmedizinische Fragestellungen. Im Rahmen der aktuellen Impfkampagne gegen Covid-19 arbeitet sie in den drei Impfzentren Bad Oldesloe, Reinbek und Großhansdorf im Kreis Stormarn in Schleswig-Holstein. Sie ist 42 Jahre alt und lebt mit ihrem Mann und ihren drei Kindern in Hamburg.